Изоэлектрическая точка, как и молекулярная масса, является одной из важнейних характеристик белка или пептида. Под изоэлектрической точкой (pI) подразумевают значение pH среды, при котором суммарный электрический заряд на поверхности белковой частицы равен нулю. Как известно, в состав белков и пептидов входят аминокислоты, содержащие как группировки, способные в водной среде отдавать протоны с возникновением отрицательного заряда (анионогенные группы), так и группировки, способные присоединять протоны с появлением положительного заряда (катионогенные группы). От соотношения тех и других зависит величина изоэлектрической точки. Если в составе белка (пептида) преобладают боковые радикалы, содержащие анионогенные группы, то его pI находится в кислой среде, где избыток протонов будет подавлять диссоциацию этих групп. Если в составе белка (пептида) преобладают боковые радикалы, содержащие катионогенные группы, то его pI находится в щелочной среде, так как протонирование этих групп будет затруднено при низкой концентрации ионов водорода в растворе.
Наличие заряда на поверхности белковой частицы является (наряду с гидратной оболочкой) одним из факторов, удерживающих белок в водных растворах. В изоэлектрической точке растворимость белка в воде минимальна и он легко выпадает в осадок при воздействиях, снижающих гидратацию его молекул (при добавлении электролитов или водоотнимающих реагентов). Это можно использовать для избирательного осаждения белков из раствора с последующей очисткой их от низкомолекулярных примесей. Зная изоэлектрическую точку определённого белка, можно предсказать направление его движения в электрическом поле при известном значении pH среды. Я уже давно вывел следующее нехитрое правило: нужно из значения pI вычесть значение pH, при котором проводится электрофорез; если в результате получается отрицательное число, то заряд белка '-' и он будет двигаться к аноду, если получается положительное число – заряд белка '+' и он будет двигаться к катоду.
Экспериментально определить изоэлектрическую точку белка можно следующим образом. Готовят ряд пробирок, содержащих буферный раствор с различными значениями pH, добавляют в каждую раствор исследуемого белка, перемешивают и наблюдают за содержимым пробирок. pH пробирки с наибольшей мутностью соответствует изоэлектрической точке.
Значение изоэлектрической точки можно также вычислить, используя специальные формулы, если известен аминокислотный состав белка или пептида. В настоящее время для подобных расчётов используются компьютерные программы. Так, например, на сайте «Практическая молекулярная биология» (http://molbiol.ru/) имеется раздел, на котором собрано большое количество программ, написанных на JavaScript. Эти программы позволяют автоматизировать многие расчёты, которые приходится производить в лабораторной практике. Среди них есть и программа «Анализ последовательности белка» (авторы – В.Клименков, А.Широкая, А.Авдей), позволяющая получить целый ряд параметров пептида или белка, исходя из его первичной структуры.
Посмотрим, как работает эта программа. В качестве примера можно взять биологически активный пептид ангиотензин II, обладающий мощным сосудосуживающим действием. Его первичная структура: Asp-Arg-Val-Tyr-Ile-His-Pro-Phe (Овчинников Ю.А. Биоорганическая химия. – М.: Просвещение, 1982, с.272).
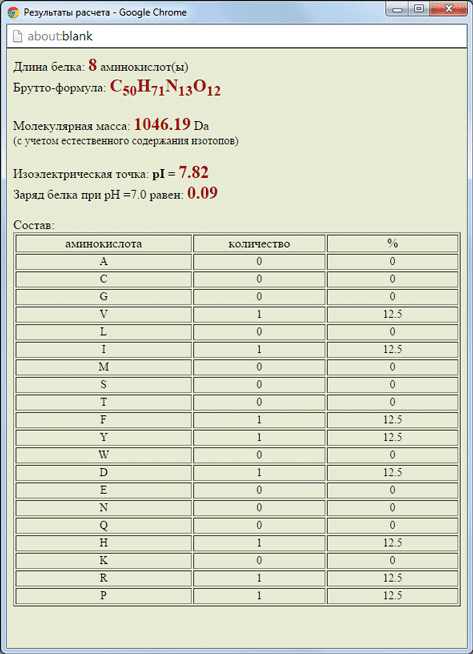
Сначала нужно перевести трёхбуквенные обозначения аминокислот пептида в однобуквенный код. Воспользуемся для этого другой программой на сайте MolBiol.ru. Полученную последовательность DRVYIHPF копируем в строку в программе «Анализ последовательности белка», нажимаем кнопку “Расчёт!” и в новом окне получаем следующую информацию:
Таким образом, изоэлектрическая точка ангиотензина II находится в слабощелочной среде, и при нейтральном значении pH данный пептид будет заряжен положительно. Можете попытаться использовать эту программу для расчёта параметров других пептидов, первичная структура которых приведена в учебнике Овчинникова.


хрень какая-то, смысловой нагрузки 2 предложения
ОтветитьУдалитьЗдравствуйте, администратор блога, я просто хочу оставить это сообщение здесь, в вашем блоге, чтобы сообщить всем о финансовой поддержке, которую г-н Бенджамин предлагает мне во время covid-19, потому что это время было действительно тяжелым и тяжелым временем для меня после блокировки страны. чуть не потерял свой бизнес до того, как Бенджамин кредитный офицер, который помог мне с ссудой по ставке 2 в обмен на финансирование моего бизнеса, я так благодарен и выражая благодарность его поддержке, я буду свидетельствовать, насколько я благодарен его служению и его работе После посещения их офиса в моем местонахождении я знал, что он был хорошим человеком с большим сердцем. Я хотел бы, чтобы кто-нибудь здесь, испытывающий финансовые затруднения, связался с мистером Бенджамином по его электронной почте 247officedept@gmaill.com, и он поможет вам с любым типом ссуд, если вы достаточно честны, чтобы вернуть деньги.
ОтветитьУдалить